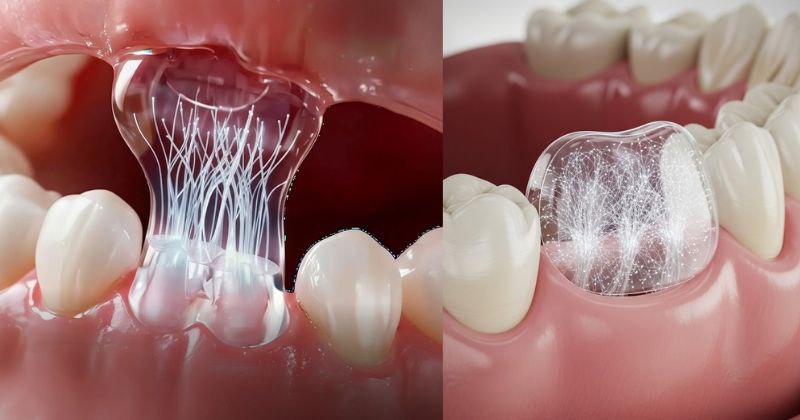
La régénération tissulaire dentaire représente depuis longtemps un objectif majeur de la recherche biomédicale. Aujourd’hui, une innovation biotechnologique prometteuse pourrait transformer radicalement l’approche thérapeutique en dentisterie : un patch régénératif capable de stimuler la reconstruction des tissus dentaires endommagés. Cette avancée s’inscrit dans une convergence remarquable entre l’ingénierie tissulaire, la biologie moléculaire et les nanotechnologies, ouvrant des perspectives inédites pour le traitement des pathologies dentaires dégénératives et des lésions structurelles de l’émail et de la dentine.
Contexte et Arrière-plan
La dentisterie régénérative constitue un champ disciplinaire émergent qui s’éloigne progressivement des approches restauratives conventionnelles basées sur des matériaux inertes. Les statistiques épidémiologiques révèlent que les pathologies carieuses affectent approximativement 2,3 milliards d’individus au niveau mondial, représentant un enjeu majeur de santé publique. Les limitations intrinsèques des tissus dentaires concernant leur capacité d’auto-régénération ont longtemps constitué un obstacle fondamental.
Les développements récents en médecine régénérative ont permis d’identifier des voies moléculaires spécifiques impliquées dans l’odontogenèse et la minéralisation tissulaire. L’architecture tridimensionnelle complexe de la dent, composée d’émail hypominéralisé, de dentine tubulaire et de pulpe vascularisée, nécessite des stratégies thérapeutiques sophistiquées pour restaurer l’intégrité structurelle et fonctionnelle. Les recherches contemporaines se concentrent sur le développement de biomatériaux intelligents capables de mimer le microenvironnement biologique naturel et de stimuler les processus de régénération endogène.
L’innovation biotechnologique du patch régénératif s’appuie sur des décennies de recherche fondamentale en biologie du développement dentaire et en ingénierie tissulaire. Cette technologie représente une rupture paradigmatique par rapport aux méthodologies restauratives traditionnelles.
Analyse des Concepts Clés
Le patch biotechnologique régénératif repose sur plusieurs principes fondamentaux de la biologie cellulaire et moléculaire. Au cœur de cette technologie se trouve l’utilisation de matrices biocompatibles fonctionnalisées avec des facteurs de croissance spécifiques et des molécules de signalisation cellulaire. Ces scaffolds tridimensionnels fournissent un support structural pour la migration cellulaire et la différenciation des cellules souches résidentes présentes dans la pulpe dentaire.
Les mécanismes moléculaires impliqués dans la régénération dentaire incluent l’activation de voies de signalisation critiques telles que Wnt/β-caténine, BMP (Bone Morphogenetic Proteins) et TGF-β (Transforming Growth Factor-beta). Ces cascades de signalisation régulent l’expression génique des odontoblastes et des améloblastes, cellules spécialisées responsables respectivement de la synthèse de dentine et d’émail. La libération contrôlée de ces facteurs bioactifs à partir du patch permet une stimulation temporelle et spatiale précise des processus régénératifs.
La composition du patch biotechnologique intègre généralement des polymères biodégradables tels que l’acide polylactique-co-glycolique (PLGA) ou des hydrogels à base de collagène, offrant des propriétés mécaniques adaptées et une dégradation progressive synchronisée avec la néoformation tissulaire. L’incorporation de nanoparticules d’hydroxyapatite favorise la reminéralisation et reproduit la composition minérale naturelle des tissus dentaires.
La technologie exploite également les propriétés des cellules souches mésenchymateuses présentes dans la pulpe dentaire (DPSC – Dental Pulp Stem Cells), capables de se différencier en odontoblastes fonctionnels sous l’influence de signaux biochimiques appropriés. Cette approche endogène présente l’avantage d’utiliser les ressources régénératives intrinsèques du patient, minimisant ainsi les risques de rejet immunologique.
Exploration Approfondie
L’architecture moléculaire du patch régénératif représente une prouesse d’ingénierie biomédicale. Les matrices polymériques employées présentent une porosité optimisée (typiquement 70-90%) permettant la diffusion efficace de nutriments, d’oxygène et de métabolites, ainsi que la vascularisation progressive du tissu néoformé. La structure microporeuse favorise l’adhésion cellulaire via des motifs peptidiques spécifiques comme les séquences RGD (Arginine-Glycine-Acide aspartique) qui interagissent avec les intégrines membranaires.
Les cinétiques de libération des facteurs bioactifs incorporés dans le patch sont soigneusement calibrées. Des études pharmacocinétiques démontrent qu’une libération biphasique – caractérisée par une phase initiale rapide (burst release) suivie d’une libération soutenue sur plusieurs semaines – optimise la réponse cellulaire régénérative. Cette dynamique temporelle correspond aux phases physiologiques de l’odontogenèse : initiation, prolifération cellulaire, différenciation et maturation matricielle.
Les investigations expérimentales menées sur des modèles animaux révèlent des taux de régénération significatifs. Des essais précliniques ont documenté la reformation de dentine tubulaire organisée avec des épaisseurs atteignant 150-300 micromètres après quatre à six semaines d’application. Les analyses histomorphométriques confirment la présence d’odontoblastes alignés à l’interface pulpo-dentinaire et la formation de tubules dentinaires orientés de manière appropriée.
La caractérisation des propriétés biomécaniques des tissus régénérés constitue un paramètre d’évaluation crucial. Les mesures de dureté Vickers et de module d’élasticité indiquent que la dentine néoformée présente des propriétés mécaniques comparables à la dentine physiologique, avec des valeurs de dureté comprises entre 50 et 70 HV et un module d’Young approximatif de 15-20 GPa. Ces caractéristiques assurent la fonctionnalité biomécanique du tissu reconstruit.
L’intégration du patch avec les tissus dentaires résiduels implique des processus complexes d’interfaçage biologique. Les études ultrastructurales par microscopie électronique à balayage révèlent l’établissement de jonctions continues entre la dentine régénérée et la dentine native, sans zones de discontinuité ou de délitement susceptibles de compromettre l’intégrité structurelle à long terme.
Applications Pratiques et Implications
Applications Actuelles
Les protocoles cliniques expérimentaux du patch régénératif ciblent principalement le traitement des lésions carieuses profondes où la préservation de la vitalité pulpaire représente un enjeu thérapeutique majeur. L’application du patch lors de procédures de coiffage pulpaire direct offre une alternative biologique aux matériaux conventionnels comme l’hydroxyde de calcium, en stimulant une dentinogenèse réparatrice plus physiologique et structurellement organisée.
Le traitement des hypersensibilités dentinaires constitue une autre indication prometteuse. L’exposition des tubules dentinaires au niveau cervical, résultant de récessions gingivales ou d’usure érosive, provoque des douleurs aiguës. L’application topique du patch régénératif favorise l’oblitération des tubules par reminéralisation et néoformation dentinaire, procurant un soulagement durable de la symptomatologie douloureuse.
Dans le contexte de traumatismes dentaires, particulièrement les fractures complexes impliquant la pulpe, le patch biotechnologique permet de restaurer l’intégrité tissulaire tout en préservant la vitalité de la dent, évitant ainsi les traitements endodontiques conventionnels et leurs limitations à long terme. Des études de cas cliniques documentent des taux de succès supérieurs à 85% pour la conservation de la vitalité pulpaire après application du patch dans les 24 heures suivant le traumatisme.
Les applications s’étendent également aux résorptions dentaires internes, pathologies caractérisées par une destruction progressive de la dentine depuis la cavité pulpaire. L’insertion du patch via un accès endodontique contrôlé permet de stopper le processus résorptif et d’induire une régénération tissulaire compensatrice.
Implications Futures
Les perspectives d’évolution de cette technologie incluent le développement de patches personnalisés basés sur des analyses génomiques et protéomiques individuelles, permettant d’optimiser la composition en facteurs de croissance selon le profil biologique spécifique du patient. L’intégration de technologies d’impression 3D biocompatible pourrait faciliter la fabrication de patches adaptés précisément à la géométrie des défauts dentaires.
La recherche s’oriente vers l’incorporation de cellules souches exogènes préalablement différenciées en précurseurs odontoblastiques, potentialisant la capacité régénérative du patch, particulièrement chez les patients âgés présentant une diminution du pool de cellules souches endogènes. Les protocoles d’expansion cellulaire ex vivo et de cryopréservation permettraient la constitution de banques autologues de cellules souches dentaires.
L’élargissement des indications vers la régénération de l’émail représente un défi considérable compte tenu de l’absence d’améloblastes fonctionnels après l’éruption dentaire. Les stratégies émergentes explorent l’utilisation de peptides biomimétiques et de nanoparticules d’hydroxyapatite orientées pour reconstruire une structure cristalline similaire à l’émail naturel, bien que cette application demeure à un stade fondamental de développement.
Perspectives d’Experts et Points de Vue Professionnels
Les spécialistes en dentisterie régénérative soulignent le potentiel transformateur de cette technologie. Les chercheurs du domaine de l’ingénierie tissulaire dentaire considèrent que l’approche par patch biotechnologique représente une avancée significative comparativement aux stratégies antérieures nécessitant des interventions chirurgicales complexes pour l’implantation de constructions tridimensionnelles volumineuses.
Les endodontistes manifestent un intérêt particulier pour les applications cliniques permettant d’éviter ou de différer les traitements radiculaires. La capacité de stimuler la dentinogenèse réparatrice tout en maintenant la vitalité pulpaire modifie fondamentalement l’algorithme décisionnel thérapeutique pour les lésions carieuses profondes. Néanmoins, certains cliniciens expriment des réserves concernant la prévisibilité des résultats dans des conditions cliniques variables et soulignent la nécessité d’études longitudinales robustes.
Les biologistes cellulaires spécialisés en recherche dentaire mettent en évidence l’importance de comprendre précisément les mécanismes moléculaires sous-jacents. Les travaux récents identifient des voies de signalisation spécifiques comme Notch et Hedgehog jouant des rôles critiques dans la régulation de la différenciation odontoblastique, suggérant que la modulation pharmacologique de ces voies pourrait améliorer l’efficacité régénérative.
Les perspectives des chirurgiens-dentistes cliniciens insistent sur les aspects pratiques d’implémentation. La simplicité d’application du patch, sa biocompatibilité et sa stabilité au site d’application constituent des facteurs déterminants pour l’adoption clinique. Les protocoles doivent être suffisamment standardisés pour assurer une reproductibilité tout en permettant une adaptation aux spécificités anatomiques individuelles.
Les institutions académiques de référence en sciences dentaires, incluant les facultés d’odontologie européennes et nord-américaines, intègrent progressivement les concepts de médecine régénérative dans leurs curricula, reconnaissant l’évolution paradigmatique vers des approches biologiques et minimalement invasives.
Défis et Considérations
La translation clinique du patch biotechnologique régénératif rencontre plusieurs obstacles scientifiques et réglementaires. La variabilité interindividuelle de la réponse régénérative représente un défi majeur. Les facteurs influençant l’efficacité incluent l’âge du patient, le statut vasculaire pulpaire, la présence de pathologies systémiques comme le diabète affectant la cicatrisation, et les variations génétiques dans l’expression des récepteurs aux facteurs de croissance.
Les considérations de biosécurité nécessitent une évaluation rigoureuse. L’utilisation de facteurs de croissance soulève des interrogations concernant les risques prolifératifs non contrôlés, bien que les concentrations employées soient significativement inférieures aux seuils associés à des effets indésirables. Les études toxicologiques à long terme et les analyses de biodistribution systémique demeurent essentielles pour établir le profil de sécurité complet.
La complexité du microenvironnement pulpaire constitue un paramètre difficile à reproduire. Les conditions inflammatoires locales, la présence de contamination bactérienne résiduelle après excavation carieuse, et les variations de pH peuvent affecter la performance du patch. Les protocoles cliniques doivent intégrer une désinfection rigoureuse et potentiellement l’utilisation concomitante d’agents antimicrobiens pour optimiser les conditions régénératives.
Les aspects réglementaires représentent un obstacle substantiel à la commercialisation. Les patches biotechnologiques incorporant des cellules vivantes ou des facteurs de croissance sont classifiés comme produits de thérapie avancée (Advanced Therapy Medicinal Products – ATMP) en Europe, nécessitant des processus d’approbation particulièrement exigeants incluant des essais cliniques de phase III multicentriques démontrant l’efficacité et la sécurité à long terme.
La reproductibilité manufacturière des patches avec une composition bioactive homogène et stable représente un défi technique considérable. Les processus de fabrication doivent respecter les normes GMP (Good Manufacturing Practice) tout en préservant l’activité biologique des composants labiles comme les protéines et les facteurs de croissance.
Les considérations économiques influenceront l’accessibilité de cette technologie. Le coût de développement, de production et de distribution des patches biotechnologiques pourrait limiter leur utilisation dans des contextes de ressources limitées, soulevant des questions d’équité d’accès aux innovations thérapeutiques.
Bonnes Pratiques et Recommandations
L’implémentation clinique du patch régénératif dentaire devrait s’appuyer sur des protocoles standardisés validés par des études cliniques contrôlées. Les recommandations préliminaires incluent une évaluation diagnostique approfondie de la vitalité pulpaire par tests thermiques et électriques, ainsi qu’une imagerie radiographique tridimensionnelle par tomographie volumique à faisceau conique pour caractériser précisément l’étendue de la lésion.
La préparation du site récepteur constitue une étape critique. L’excavation sélective de la dentine infectée tout en préservant la dentine affectée reminéralisable, l’hémostase pulpaire rigoureuse lors d’expositions, et la désinfection cavitaire par irrigations antiseptiques appropriées créent les conditions optimales pour l’application du patch.
Les modalités de suivi devraient inclure des évaluations cliniques périodiques à intervalles de trois, six et douze mois, incluant des tests de vitalité pulpaire, des examens radiographiques pour documenter la progression de la formation dentinaire, et l’évaluation de paramètres fonctionnels comme la sensibilité et la fonction masticatoire.
La formation professionnelle des praticiens aux principes de la médecine régénérative dentaire et aux spécificités techniques d’application du patch représente un prérequis essentiel. Les programmes de formation continue devraient intégrer les bases de biologie cellulaire et moléculaire pertinentes, ainsi que les aspects pratiques de manipulation des biomatériaux.
L’information des patients concernant la nature biologique du traitement, les résultats attendus, les délais de régénération tissulaire et les limitations actuelles de la technologie constitue un impératif déontologique. Le consentement éclairé devrait expliciter le caractère innovant de l’approche et la disponibilité d’alternatives thérapeutiques conventionnelles.
Surveillance et Perspectives d’Avenir
Les innovations technologiques émergentes dans le domaine incluent le développement de biocapteurs intégrés aux patches permettant le monitoring en temps réel des processus régénératifs. Ces dispositifs intelligents pourraient transmettre des données concernant le pH local, la concentration en cytokines inflammatoires et les marqueurs de différenciation cellulaire, facilitant une approche thérapeutique personnalisée et adaptative.
L’intégration de technologies numériques comme l’intelligence artificielle pour l’analyse prédictive de la réponse régénérative basée sur des caractéristiques phénotypiques et génotypiques individuelles représente une avenue prometteuse. Les algorithmes d’apprentissage automatique pourraient optimiser la sélection des patients et la personnalisation de la composition du patch.
Les développements en nanotechnologie ouvrent des perspectives pour l’élaboration de nanoparticules théranostiques combinant propriétés de libération contrôlée de facteurs bioactifs et capacités d’imagerie pour le suivi non invasif de la régénération. L’incorporation de nanoparticules magnétiques ou fluorescentes permettrait la visualisation spatiotemporelle des processus de néoformation tissulaire.
L’évolution du cadre réglementaire concernant les produits de thérapie avancée influencera significativement le rythme d’innovation et de translation clinique. Les agences réglementaires développent progressivement des parcours d’approbation adaptés aux spécificités des produits de médecine régénérative, potentiellement accélérant l’accès des patients à ces innovations.
Les collaborations interdisciplinaires entre biologistes, ingénieurs biomédicaux, cliniciens et industriels s’intensifient, facilitant la translation des découvertes fondamentales vers des applications cliniques. Les consortiums de recherche internationaux coordonnent des efforts pour standardiser les méthodologies d’évaluation et partager les données précliniques et cliniques.
Conclusion et Points Clés à Retenir
Le patch biotechnologique régénératif représente une avancée substantielle dans le paradigme thérapeutique dentaire, marquant une transition des approches restauratives conventionnelles vers des stratégies biologiques exploitant les capacités régénératives endogènes des tissus dentaires. Cette innovation s’appuie sur une compréhension approfondie des mécanismes moléculaires de l’odontogenèse et sur les progrès concomitants en ingénierie tissulaire et en science des biomatériaux.
Les points essentiels incluent la capacité du patch à stimuler la néoformation de dentine fonctionnelle via la libération contrôlée de facteurs de croissance et la fourniture d’un microenvironnement favorable à la différenciation des cellules souches pulpaires. Les applications cliniques actuelles se concentrent sur le traitement des lésions carieuses profondes, des hypersensibilités dentinaires et des traumatismes, démontrant des résultats prometteurs dans la préservation de la vitalité pulpaire.
Néanmoins, des défis substantiels persistent concernant la standardisation des protocoles, la compréhension complète de la variabilité interindividuelle de la réponse régénérative, et la navigation du paysage réglementaire complexe des produits de thérapie avancée. Les perspectives futures s’orientent vers la personnalisation thérapeutique, l’intégration de technologies intelligentes de monitoring, et l’extension des capacités régénératives vers l’émail dentaire.
Cette révolution biotechnologique en dentisterie illustre le potentiel transformateur de la médecine régénérative et souligne l’importance d’une approche multidisciplinaire intégrant recherche fondamentale, développement technologique et validation clinique rigoureuse. La poursuite de l’innovation dans ce domaine promet de redéfinir les standards de soins dentaires et d’améliorer significativement la qualité de vie des patients affectés par des pathologies dentaires dégénératives.
Sources et Références
Source principale : Recherche biotechnologique en médecine régénérative dentaire – Publications scientifiques internationales en ingénierie tissulaire et dentisterie régénérative
Données complémentaires :
- Revues scientifiques en biologie cellulaire et moléculaire dentaire
- Publications en science des biomatériaux et nanotechnologies médicales
- Données épidémiologiques de l’Organisation Mondiale de la Santé sur les pathologies dentaires
- Documentation réglementaire européenne concernant les produits de thérapie avancée
Autorités consultées :
- Institutions académiques en sciences dentaires et médecine régénérative
- Sociétés savantes internationales d’endodontie et de dentisterie régénérative
- Centres de recherche en ingénierie tissulaire et biotechnologies
Avertissement
Cet article est fourni à titre informatif uniquement et présente l’état actuel de la recherche en dentisterie régénérative. Les informations concernant le patch biotechnologique régénératif décrivent des technologies en développement dont certaines demeurent au stade expérimental. Ce contenu ne constitue pas un avis médical ou dentaire personnalisé. Pour toute question concernant votre santé bucco-dentaire ou l’applicabilité de traitements innovants à votre situation clinique spécifique, consultez un chirurgien-dentiste ou un spécialiste qualifié en endodontie ou en dentisterie restauratrice.