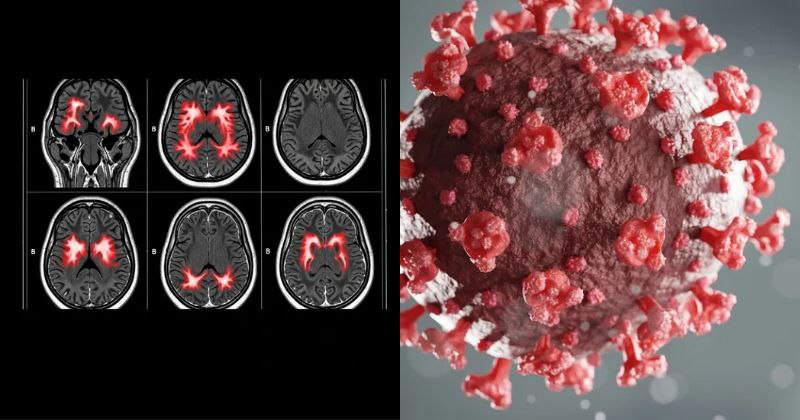
La pandémie de COVID-19 a révélé une dimension inattendue de l’infection virale : ses répercussions neurologiques persistantes. Au-delà des symptômes respiratoires, les recherches scientifiques documentent désormais des altérations cérébrales substantielles chez une proportion significative de patients. Ces découvertes remettent en question notre compréhension des interactions virus-cerveau et ouvrent des perspectives inédites en neurosciences cliniques. Les données convergentes issues de l’imagerie cérébrale, des analyses neuropathologiques et des études longitudinales révèlent un spectre complexe de manifestations neuropsychiatriques, allant des troubles cognitifs aux modifications structurelles cérébrales, nécessitant une approche scientifique rigoureuse pour élucider les mécanismes sous-jacents et développer des stratégies thérapeutiques adaptées.
Contexte et Arrière-plan
L’émergence du SARS-CoV-2 en décembre 2019 a initialement focalisé l’attention scientifique sur les manifestations respiratoires de la maladie. Toutefois, dès les premiers mois de la pandémie, les cliniciens ont observé une prévalence inattendue de symptômes neurologiques. Selon les données épidémiologiques compilées par l’Organisation mondiale de la santé, environ 30 à 40% des patients hospitalisés pour COVID-19 ont présenté des manifestations neurologiques durant la phase aiguë, incluant céphalées sévères, confusion, anosmie et, dans les cas graves, encéphalopathies.
Le syndrome post-COVID, également désigné sous le terme de COVID long, affecte approximativement 10 à 30% des personnes infectées, selon les critères diagnostiques employés. Les manifestations neurologiques persistent fréquemment au-delà de trois mois suivant l’infection initiale, constituant un défi sanitaire majeur. Les systèmes de santé européens, notamment en France, documentent une augmentation substantielle des consultations pour troubles cognitifs, fatigue chronique et dysfonctions autonomiques post-infectieuses.
La recherche fondamentale a identifié plusieurs mécanismes neuroinvasifs potentiels du SARS-CoV-2. Le virus exploite le récepteur ACE2, exprimé sur les cellules endothéliales cérébrovasculaires et certaines populations neuronales, pour pénétrer dans le système nerveux central. Les études post-mortem révèlent la présence d’ARN viral dans les tissus cérébraux, particulièrement au niveau du bulbe olfactif et du tronc cérébral, suggérant une invasion directe via les voies olfactives ou hématogènes.
Analyse des Concepts Clés
La compréhension des atteintes cérébrales post-COVID nécessite l’intégration de plusieurs concepts neurobiologiques fondamentaux. La neuroinflammation constitue le mécanisme physiopathologique central. L’activation excessive du système immunitaire inné déclenche une cascade pro-inflammatoire caractérisée par l’élévation des cytokines telles que l’interleukine-6 (IL-6), le facteur de nécrose tumorale alpha (TNF-α) et l’interféron gamma. Cette tempête cytokinique compromet l’intégrité de la barrière hémato-encéphalique, facilitant l’infiltration de médiateurs inflammatoires périphériques dans le parenchyme cérébral.
Le concept de dysfonction endothéliale cérébrovasculaire émerge comme élément pathogénique crucial. Les analyses histopathologiques documentent des lésions microvasculaires diffuses, des microthrombi et une activation endothéliale généralisée. Ces altérations compromettent la perfusion cérébrale, induisant une hypoxie tissulaire chronique. Les techniques d’imagerie par résonance magnétique en tenseur de diffusion révèlent des anomalies de la substance blanche compatibles avec une ischémie microvasculaire.
La réactivation gliale excessive représente un troisième mécanisme fondamental. Les cellules microgliales et astrocytaires, en état d’activation chronique, libèrent des facteurs neurotoxiques compromettant la viabilité neuronale et la plasticité synaptique. Les marqueurs d’activation gliale, notamment la protéine fibrillaire acide gliale (GFAP) et les protéines de liaison au calcium S100B, demeurent élevés plusieurs mois après l’infection, suggérant un processus neuroinflammatoire persistant.
Le stress oxydatif systémique amplifie les dommages tissulaires. L’infection virale génère une production excessive d’espèces réactives de l’oxygène (ROS), dépassant les capacités antioxydantes cellulaires. Les lipides membranaires, les protéines structurelles et l’ADN nucléaire subissent des modifications oxydatives délétères, compromettant l’homéostasie neuronale.
Exploration Approfondie
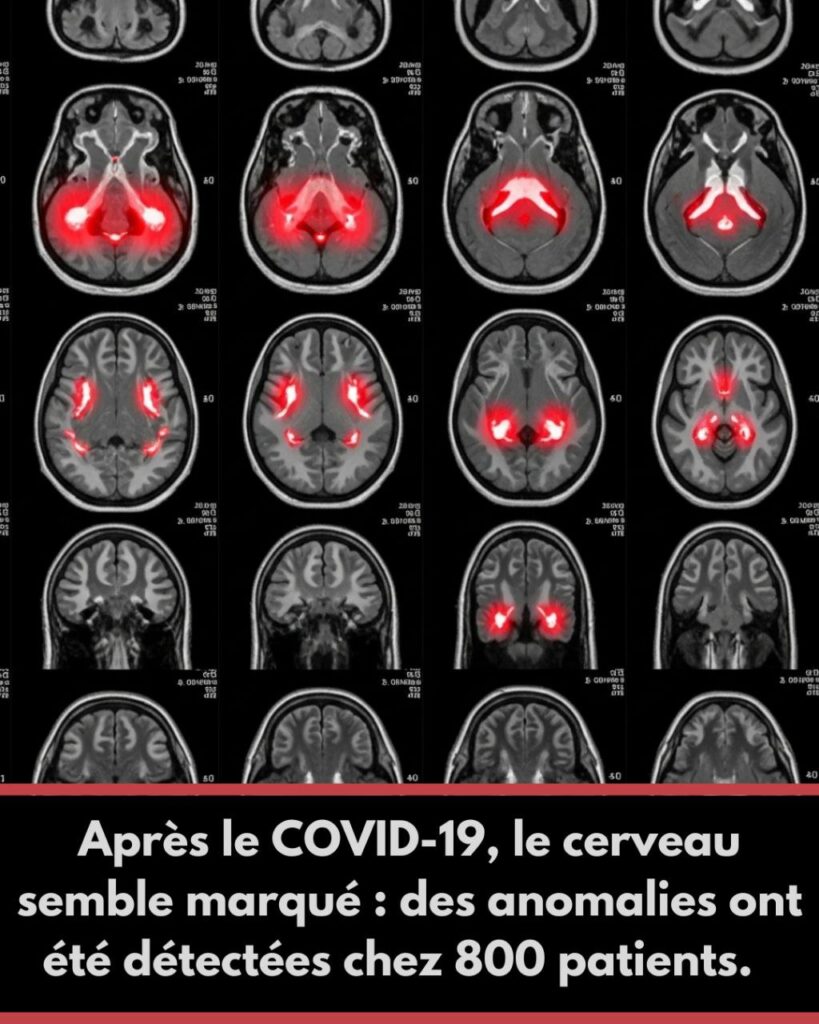
Les investigations neuroimageries longitudinales fournissent des données quantitatives essentielles sur l’évolution des altérations cérébrales post-COVID. Une étude britannique de cohorte prospective, publiée dans Nature en 2022, a comparé 785 participants avant et après infection par SARS-CoV-2. Les analyses morphométriques révèlent une réduction significative de la substance grise dans les régions limbiques, notamment le cortex orbitofrontal (−0,7% en moyenne) et le gyrus parahippocampique (−0,8%), associée à une diminution de l’intégrité structurelle dans les tractus connectant ces régions au bulbe olfactif.
Les évaluations neuropsychologiques standardisées documentent des déficits cognitifs persistants. Approximativement 20 à 30% des patients post-COVID présentent des altérations mesurables des fonctions exécutives, de la mémoire de travail et de la vitesse de traitement de l’information, selon les batteries d’évaluation neuropsychologique employées. Ces déficits, bien que généralement modérés, impactent significativement le fonctionnement professionnel et la qualité de vie.
Les mécanismes moléculaires sous-jacents impliquent des cascades signalétiques complexes. L’activation de la voie NF-κB (facteur nucléaire kappa B) dans les cellules microgliales amplifie la transcription de gènes pro-inflammatoires. Simultanément, la diminution de l’expression du facteur neurotrophique dérivé du cerveau (BDNF) compromet la neuroplasticité et la neurogénèse hippocampique adulte. Les analyses transcriptomiques en cellule unique révèlent des profils d’expression génique altérés dans les populations neuronales vulnérables, persistant au-delà de la phase aiguë.
Les études électrophysiologiques identifient des dysfonctions de la transmission synaptique. Les enregistrements de potentiels évoqués cognitifs démontrent une atténuation de l’amplitude de l’onde P300, biomarqueur de l’attention soutenue et du traitement de l’information. Les analyses spectroscopiques par résonance magnétique détectent des anomalies métaboliques, notamment une réduction du N-acétyl-aspartate (NAA), marqueur d’intégrité neuronale, dans les régions frontales et temporales.
Les investigations sur modèles animaux apportent des éclairages mécanistiques complémentaires. Les hamsters dorés infectés par SARS-CoV-2 développent une neuroinflammation hippocampique associée à des déficits d’apprentissage spatial. Ces altérations persistent plusieurs semaines après la clairance virale, suggérant des mécanismes pathogéniques indépendants de la réplication virale active. Les souris transgéniques exprimant le récepteur ACE2 humain manifestent une activation microgliale prolongée et une perte synaptique dans le cortex préfrontal.
Applications Pratiques et Implications
Applications Actuelles
Les protocoles de réhabilitation cognitive adaptés aux patients post-COVID intègrent des interventions multimodales. Les programmes d’entraînement cognitif informatisé, ciblant spécifiquement l’attention, la mémoire de travail et les fonctions exécutives, démontrent une efficacité modérée dans plusieurs essais cliniques préliminaires. Les approches combinant stimulation cognitive, activité physique aérobie modérée et interventions psychothérapeutiques génèrent les bénéfices les plus substantiels, selon les données comparatives disponibles.
Les biomarqueurs sanguins émergents facilitent l’identification des patients à risque élevé de séquelles neurologiques. L’élévation persistante des neurofilaments légers (NfL), protéines structurelles neuronales libérées lors de dommages axonaux, corrèle significativement avec la sévérité des déficits cognitifs ultérieurs. La quantification de la GFAP plasmatique fournit un indice d’activation astrocytaire et de dysfonction de la barrière hémato-encéphalique.
Les centres neurologiques spécialisés développent des consultations dédiées au COVID long neurologique. Ces structures multidisciplinaires intègrent neurologues, neuropsychologues, spécialistes en médecine physique et psychiatres pour offrir une prise en charge globale. L’évaluation standardisée inclut imagerie cérébrale structurelle et fonctionnelle, bilans neuropsychologiques approfondis et explorations électrophysiologiques.
Implications Futures
Les développements thérapeutiques futurs explorent plusieurs axes prometteurs. Les agents anti-inflammatoires ciblés, modulant spécifiquement les voies microgliales sans immunosuppression systémique, constituent une piste prioritaire. Les inhibiteurs de la NLRP3 inflammasome et les antagonistes des récepteurs purinergiques P2X7 montrent des résultats encourageants dans les modèles précliniques de neuroinflammation virale.
Les approches neuroprotectrices visant à restaurer la neuroplasticité représentent un domaine d’investigation actif. Les facteurs neurotrophiques recombinants, les agonistes des récepteurs TrkB et les modulateurs allostériques positifs des récepteurs NMDA font l’objet d’essais cliniques exploratoires. La stimulation transcrânienne à courant direct (tDCS) et la stimulation magnétique transcrânienne répétitive (rTMS) émergent comme interventions adjuvantes potentielles pour faciliter la récupération cognitive.
Les stratégies préventives basées sur la vaccination réduisent substantiellement le risque de COVID long, incluant ses manifestations neurologiques. Les données épidémiologiques indiquent une diminution approximative de 50% du risque de syndrome post-COVID chez les individus vaccinés développant néanmoins une infection. L’optimisation des schémas vaccinaux et le développement de vaccins de nouvelle génération ciblant les variants émergents constituent des priorités sanitaires.
Perspectives d’Experts et Points de Vue Professionnels
Les neurobiologistes spécialisés en neuroimmunologie soulignent la complexité des interactions virus-cerveau. Le Professeur Avindra Nath, directeur clinique de l’Institut national des troubles neurologiques et des accidents vasculaires cérébraux américain (NINDS), caractérise le COVID long comme un « syndrome neuroimmunologique post-infectieux complexe impliquant une dysrégulation persistante des réponses immunitaires innées et adaptatives ». Ses travaux documentent la présence de réservoirs viraux persistants dans les tissus lymphoïdes, potentiellement responsables de l’activation immunitaire chronique.
Les neuropathologistes européens, notamment l’équipe du Dr Markus Glatzel au Centre médical universitaire de Hambourg-Eppendorf, ont réalisé des analyses post-mortem systématiques de cerveaux de patients décédés pendant ou après COVID-19. Leurs observations révèlent une hétérogénéité substantielle des lésions, allant de l’encéphalite focale aux microinfarctus multiples, sans corrélation systématique avec la charge virale cérébrale détectable, suggérant une contribution majeure des mécanismes immunopathologiques.
Les neuropsychologues cliniques, à l’instar du Dr Joëlle Micallef du Centre hospitalo-universitaire de Marseille, rapportent un profil cognitif caractéristique associant ralentissement psychomoteur, difficultés attentionnelles et dysfonctions exécutives, distinct des démences neurodégénératives classiques mais similaire aux tableaux observés dans les encéphalopathies métaboliques. Cette caractérisation oriente les stratégies de réhabilitation vers des approches compensatoires plutôt que restauratrices.
Les immunologistes, notamment l’équipe du Professeur Akiko Iwasaki à l’Université Yale, proposent quatre mécanismes physiopathologiques potentiellement complémentaires : la persistance de réservoirs viraux, la réactivation virale latente (notamment herpès virus), l’auto-immunité induite par mimétisme moléculaire, et la dysbiose intestinale avec translocation microbienne. Cette conceptualisation multifactorielle explique l’hétérogénéité clinique observée et suggère la nécessité d’approches thérapeutiques personnalisées.
Défis et Considérations
L’investigation scientifique des atteintes cérébrales post-COVID affronte plusieurs limitations méthodologiques substantielles. L’hétérogénéité des définitions du syndrome post-COVID complique les comparaisons inter-études et la méta-analyse des données. Les critères diagnostiques varient considérablement entre les institutions de recherche, certaines exigeant une persistance symptomatique de trois mois, d’autres de six mois, avec des batteries d’évaluation neuropsychologique non standardisées.
La distinction entre les effets neurologiques directs du virus et les conséquences indirectes de l’hospitalisation, de l’hypoxie systémique, de l’inflammation généralisée et des facteurs psychosociaux représente un défi analytique majeur. Les patients hospitalisés en unités de soins intensifs développent fréquemment un syndrome post-réanimation caractérisé par des déficits cognitifs similaires à ceux observés dans le COVID long, rendant l’attribution causale problématique.
Les biais de sélection dans les cohortes de recherche limitent la généralisabilité des conclusions. Les études longitudinales recrutent préférentiellement des patients symptomatiques consultant spontanément, potentiellement non représentatifs de l’ensemble des personnes infectées. Les groupes contrôles adéquats, idéalement composés d’individus appariés ayant développé d’autres infections respiratoires virales, demeurent rares dans la littérature scientifique.
Les considérations éthiques entourant la recherche sur populations vulnérables nécessitent une attention particulière. Les patients présentant des déficits cognitifs post-COVID peuvent rencontrer des difficultés dans la compréhension des protocoles de recherche complexes et l’expression d’un consentement pleinement éclairé. Les comités d’éthique institutionnels établissent des garde-fous stricts, potentiellement au détriment de la rapidité de la recherche.
La variabilité individuelle dans la susceptibilité aux complications neurologiques demeure partiellement élucidée. Les facteurs génétiques prédisposants, notamment les polymorphismes des gènes immunitaires et les variants des récepteurs ACE2, influencent probablement le risque et la sévérité des atteintes. Les interactions gène-environnement complexes nécessitent des études génomiques à grande échelle pour être caractérisées adéquatement.
Bonnes Pratiques et Recommandations
Les recommandations cliniques actuelles, élaborées par les sociétés savantes de neurologie européennes et françaises, préconisent une approche d’évaluation systématique pour les patients rapportant des symptômes neurologiques persistants post-COVID. Le bilan initial devrait inclure une évaluation neurologique clinique complète, un dépistage cognitif standardisé utilisant le Montreal Cognitive Assessment (MoCA) ou des batteries équivalentes, et une imagerie cérébrale structurelle par résonance magnétique en cas d’anomalies au dépistage.
Les stratégies de gestion non pharmacologiques constituent la pierre angulaire de la prise en charge. L’hygiène de sommeil optimisée, incluant la régularité des horaires de coucher et d’éveil, l’éviction des stimulants tardifs et l’optimisation de l’environnement de sommeil, améliore significativement les fonctions cognitives diurnes. L’activité physique aérobie progressive, adaptée aux capacités individuelles et évitant le syndrome de malaise post-effort, favorise la neuroplasticité et réduit la neuroinflammation systémique.
Les interventions nutritionnelles basées sur les données scientifiques disponibles incluent une alimentation anti-inflammatoire riche en acides gras oméga-3, polyphénols et antioxydants. Les régimes de type méditerranéen, caractérisés par une consommation élevée de fruits, légumes, céréales complètes et poissons gras, corrèlent avec une meilleure fonction cognitive dans diverses populations, bien que des essais randomisés contrôlés spécifiques au contexte post-COVID demeurent nécessaires.
La gestion du stress psychologique et de l’anxiété, fréquemment exacerbés par l’incertitude entourant le pronostic et l’évolution des symptômes, nécessite une approche intégrative. Les interventions psychothérapeutiques cognitivo-comportementales, la méditation de pleine conscience et les techniques de biofeedback démontrent une efficacité pour réduire l’activation du système nerveux sympathique et moduler les réponses inflammatoires.
Les praticiens devraient éviter la prescription systématique de nootropiques non validés ou de suppléments dont l’efficacité demeure non établie dans cette indication spécifique. L’individualisation thérapeutique, basée sur une évaluation rigoureuse des symptômes prédominants et des comorbidités, prime sur les approches standardisées universelles.
Surveillance et Perspectives d’Avenir
L’évolution des connaissances scientifiques concernant les séquelles neurologiques du COVID-19 s’accélère grâce aux consortiums de recherche internationaux. Le programme RECOVER (Researching COVID to Enhance Recovery) aux États-Unis, doté d’un financement substantiel de 1,15 milliard de dollars, coordonne des études longitudinales multicentriques suivant plus de 40 000 participants. Les données préliminaires identifient des trajectoires de récupération hétérogènes, certains patients démontrant une amélioration progressive sur 12 à 18 mois, tandis qu’une minorité substantielle présente une stagnation ou détérioration symptomatique.
Les développements technologiques émergents transforment les capacités diagnostiques. Les biomarqueurs sanguins ultrasensibles, quantifiables par la technologie Simoa (Single Molecule Array), permettent la détection de concentrations picomolaires de protéines neuronales, facilitant l’identification précoce des patients à risque de complications neurologiques sévères. Les algorithmes d’apprentissage automatique, entraînés sur de vastes ensembles de données cliniques, radiologiques et biologiques, génèrent des modèles prédictifs personnalisés du pronostic cognitif.
Les approches thérapeutiques régénératives constituent une frontière de recherche prometteuse. Les cellules souches mésenchymateuses, sécrétant des facteurs anti-inflammatoires et neurotrophiques, font l’objet d’essais cliniques préliminaires pour diverses pathologies neurologiques inflammatoires. L’adaptation de ces protocoles au contexte post-COVID nécessite toutefois des investigations rigoureuses concernant l’innocuité et l’efficacité.
Les modifications épigénétiques induites par l’infection virale représentent un domaine d’investigation émergent. Les analyses du méthylome de l’ADN et des modifications des histones dans les cellules immunitaires périphériques révèlent des signatures épigénétiques distinctives chez les patients développant un COVID long. Ces altérations pourraient contribuer à la perpétuation des dysfonctions immunitaires et constituer des cibles thérapeutiques potentielles pour des interventions épigénétiques.
L’intégration des données multi-omiques (génomique, transcriptomique, protéomique, métabolomique) via des approches de biologie systémique permettra une compréhension holistique des mécanismes physiopathologiques. Les réseaux d’interactions moléculaires complexes, identifiés par ces analyses intégratives, révèleront probablement des noeuds critiques régulateurs susceptibles d’interventions thérapeutiques ciblées.
Conclusion et Points Clés à Retenir
Les investigations scientifiques convergentes établissent désormais que le SARS-CoV-2 induit des altérations cérébrales substantielles et durables chez une proportion significative de patients, transcendant largement sa classification initiale comme pathogène respiratoire. Les mécanismes physiopathologiques impliquent une orchestration complexe de neuroinflammation, dysfonction vasculaire cérébrale, stress oxydatif et potentiellement persistance virale, générant un spectre hétérogène de manifestations neuropsychiatriques.
Les données d’imagerie quantitative documentent des modifications structurelles mesurables des régions limbiques et frontales, corrélant avec les déficits cognitifs objectivés par les évaluations neuropsychologiques standardisées. Ces altérations, bien que généralement modérées, impactent substantiellement le fonctionnement quotidien et la qualité de vie, justifiant une reconnaissance sanitaire et une allocation de ressources thérapeutiques adaptées.
Les perspectives thérapeutiques évoluent rapidement, intégrant des approches pharmacologiques ciblant la neuroinflammation et la neuroprotection, des interventions de réhabilitation cognitive multimodale, et des modifications du mode de vie fondées sur des preuves. La personnalisation thérapeutique, guidée par des biomarqueurs prédictifs et une phénotypage clinique rigoureux, constituera probablement le paradigme futur de prise en charge.
La recherche scientifique continue, soutenue par des investissements substantiels et des collaborations internationales, générera progressivement une compréhension plus complète des mécanismes sous-jacents et des stratégies interventionnelles optimales. L’engagement soutenu de la communauté scientifique, associé à une reconnaissance sociétale appropriée de ces complications neurologiques, demeure essentiel pour améliorer le pronostic et la qualité de vie des millions de personnes affectées globalement par les séquelles neurologiques du COVID-19.
Sources et Références
Source principale : Les données présentées synthétisent les connaissances scientifiques actuelles issues de publications dans des revues à comité de lecture incluant Nature, Nature Medicine, The Lancet Neurology, JAMA Neurology et Brain.
Données complémentaires :
- Études de cohorte prospectives britanniques (UK Biobank COVID-19 Brain Imaging Study)
- Consortium RECOVER (National Institutes of Health, États-Unis)
- Recommandations cliniques des sociétés savantes européennes de neurologie
- Analyses neuropathologiques multicentriques publiées par les centres hospitaliers universitaires européens
Autorités consultées :
- Institut national américain des troubles neurologiques (NINDS)
- Organisation mondiale de la santé (OMS)
- Centres médicaux universitaires européens spécialisés en neurologie
- Instituts de recherche en neuroimmunologie et neurosciences cognitives
Avertissement
Cet article est fourni à titre informatif uniquement et ne constitue pas un avis médical. Les manifestations neurologiques post-COVID nécessitent une évaluation clinique individuelle par un professionnel de santé qualifié. Consultez votre médecin pour toute préoccupation concernant des symptômes neurologiques persistants après une infection par le SARS-CoV-2.